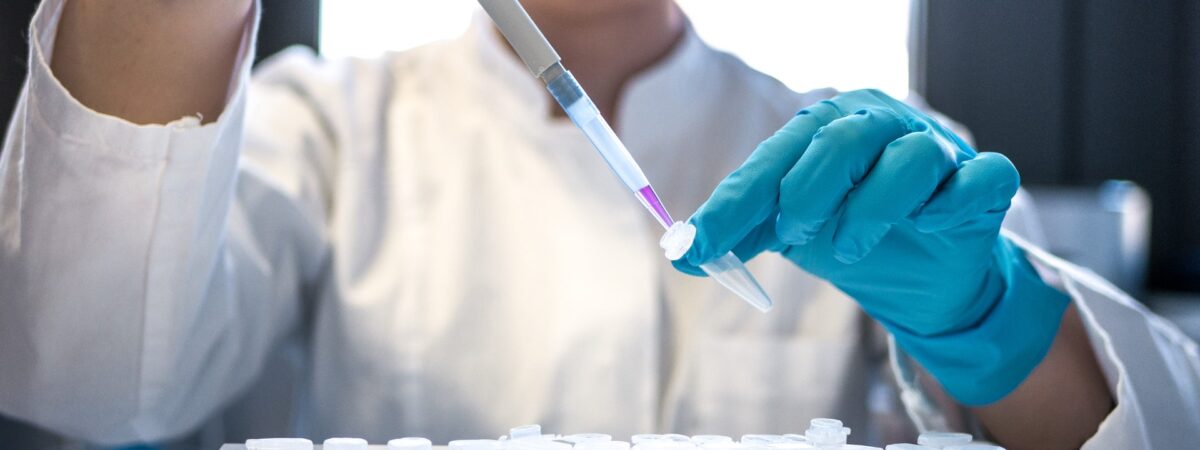
Skąd wiadomo, czy coś jest kancerogenne, czy nie? Dlaczego w sprawie jednych substancji mamy pewność, a o inne wciąż naukowcy się spierają? Jak postęp nauki wpływa na zmianę klasyfikacji? Jak dochodzi się do konsensusu – kto i jak ocenia, co jest „wystarczającym dowodem”? Czyli innymi słowy – jak funkcjonuje IARC, czyli Międzynarodowa Agencja Badań nad Rakiem?
Pewnego razu we Francji…
Międzynarodowa Agencja Badań nad Rakiem, czyli IARC (International Agency for Research on Cancer) to wyspecjalizowana agenda Światowej Organizacji Zdrowia, powołana do życia 20 maja 1965 roku (właśnie obchodzimy mało okrągłą, 57. rocznicę ;p) z inicjatywy Francji – stąd do dziś jej siedziba znajduje się w Lyonie, a francuski jest drugim językiem urzędowym po angielskim. Za historią jej powstania kryje się osobista tragedia mężczyzny, który przez tę chorobę stracił żonę – jak wielu przed nim i po nim – ale akurat Yves Poggiolli był znanym dziennikarzem, działającym we francuskiej organizacji „Ruch dla Pokoju”, powstałej po II Wojnie Światowej.
Co ważniejsze, jego redaktorem naczelnym był Emmanuel d’Astier de La Vigerie, bohater wojenny z ruchu oporu i jedna z najważniejszych postaci publicznych powojennej Francji. D’Astier, poruszony listem od Poggiolli’ego, zajął się zdobywaniem poparcia dla idei stworzenia IARC. 7 Listopada 1963 r. napisał do prezydenta Charlesa de Gaulle’a, którego dobrze znał z czasów wojny, list otwarty, sygnowany przez tuzin powszechnie szanowanych postaci publicznych powojennej Francji. Byli to, oprócz lekarzy, m.in. wybitni fizycy jak Pierre Auger (elektrony Augera) i Francis Perrin (masa neutron, naturalny reaktor jądrowy w Oklo), a także słynny architekt Charles Le Corbusier!
IARC rozpoczyna działalność 20 maja 1965 roku
Autorzy listu otwartego zaproponowali, alby „kpiarsko” małą część budżetu przeznaczonego na zbrojenia atomowe, 0,5%, przeznaczyć na tę międzynarodową instytucję. Dlatego też kopię listu przekazano do ambasady USA, UK i ZSRR, czyli ówczesnych krajów posiadających broń jądrową. Odpowiedź od de Gaulle’a przyszła po dwóch dniach, a po czterech francuski minister zdrowia, Raymond Marcellin, zadzwonił do ówczesnego szefa WHO – i nadano sprawie bieg. Zaledwie półtora roku później, po burzliwych dyskusjach na temat kształtu przyszłej organizacji wewnątrz WHO i innych instytucjach zajmujących się rakiem, IARC oficjalnie rozpoczęło działalność.
Niestety pierwotny pomysł przeznaczenia promila środków ze zbrojeń na badania przepadł, więc zamiast „miliona dolarów na dzień” nie udało się uzbierać miliona dolarów na rok. Zebrano tylko 100 tysięcy dolarów od każdego z partnerów, więc budżet i ambicje zostały okrojone, ale to nic nowego, że rządzący na całym świecie więcej pieniędzy przeznaczają na zabijanie niż leczenie…
Państwami-założycielami Komisji, oprócz Francji, był RFN, Włochy, UK i USA, w kolejnych latach do organizacji dołączyły jeszcze 22 państwa. Jej nadrzędnym celem wciąż jest koordynacja międzynarodowych badań nad rakiem, ale – co istotne – nie w kwestii terapii, a przyczyn jego występowania. Chodzi bowiem nie o leczenie, a zapobieganie jego powstawania. Zrozumienie, jakie czynniki i z jakiego powodu są kancerogenne, to podstawa do tego, by państwa mogły wdrażać prawo i procedury chroniące przed nimi obywateli. Niestety nie jest to takie proste, jakby się wydawało…
Cztery filary
W strukturze organizacyjnej IARC wyróżnione są cztery filary. Pierwszy z nich to „dane dla działania” (data for action), bo bez danych trudno mówić o Medycynie Opartej Na Dowodach. Przede wszystkim chodzi tu o nadzór nad kartotekami onkologicznymi – rzetelne zbieranie danych zgodnie z przyjętą systematyką pozwala śledzić trendy i dokonywać analiz, np. w podziale na wiek, płeć, wykonywany zawód, stosowaną dietę czy miejsce, w którym się żyje.
Zauważenie, że w danej podgrupie społecznej dany typ nowotworu występuje częściej niż w innej daje do myślenia – jest to artefakt statystyczny, czy może jest jakiś czynnik, który powoduje nowotworzenie? Analizowane czynniki (ang. Agents) mogą być czynnikami chemicznymi (dym tytoniowy…), fizycznymi (promieniowanie jonizujące…), biologicznymi (wirus HPV…), ale też związane z warunkami pracy (deprawacja snu!) czy składnikami diety (otyłość…).
Tu pojawia się filar drugi – „zrozumienie przyczyn” (understanding the causes), na który składają się grupy do epidemiologii genomicznej oraz żywienia i metabolizmu. Te grupy są w stanie wskazać, jaki jest potencjalny czynnik onkogenny, ale aby wyjaśnić dokładny mechanizm powodujący nowotworzenie oraz planować działania prewencyjne, potrzebny jest filar trzeci: „od zrozumienia do prewencji” (from understanding to prevention), na który składają się trzy grupy: „epidemiologia środowiska i stylu życia”, „epigenetyka i mechanizmy” oraz „wczesne wykrywanie, prewencja i infekcja”, które wspólnie z poprzednimi grupami wspierane są przez laboratoria i biobanki.
Na bazie tych trzech filarów może działać filar czwarty: „mobilizacja wiedzy”, w którym funkcjonuje grupa „uczenia i budowania zdolności”, organizująca transfer wiedzy choćby poprzez staże, kursy i szkolenia dla specjalistów, oraz najbliższa nam grupa „syntezy dowodów i klasyfikacji”. Najbliższa, bo to ona ostatecznie stoi za „monografiami”, czyli podstawowym i autorytatywnym źródłem wiedzy o czynnikach kancerogennych u ludzi.
Monografie – konsensus EBM
Rozpoczęty ponad pół wieku temu, w 1971 roku, program monografii odbywa się według bardzo rygorystycznych, a przede wszystkim transparentnych kryteriów opisanych we wspólnej Preambule. Definiuje ona trzy „strumienie” dowodów: badania nad ludzkimi nowotworami, eksperymenty na zwierzętach i dowody mechanicystyczne (jak opisanie ścieżki metabolicznej, w którą dany czynnik ingeruje).
Definiuje także, kiedy wyniki publikacji uznaje się za „wystarczające”, „ograniczone” lub „nieadekwatne”. Przykładowo, aby uznać rezultaty z badań na zwierzętach za „wystarczające”, to relacja przyczynowo-skutkowa musi być dowiedziona co najmniej na dwóch różnych gatunkach zwierząt lub na jednym, ale przez co najmniej dwa niezależne zespoły badawcze. Szczegóły znajdują się w tabeli:
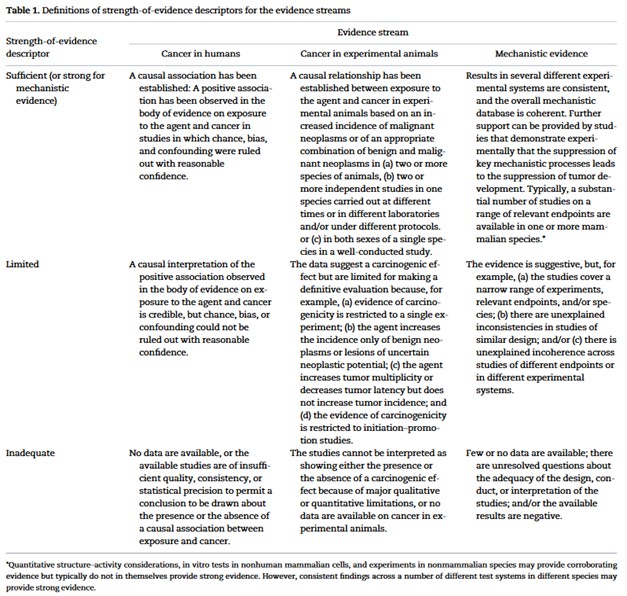
Gdy mamy do dyspozycji trzy strumienie danych, spośród których każdy jest oceniony w powyższej skali, rodzi się pytanie – co, jeśli na przykład badania na ludziach nie są (jeszcze?) przekonujące, ale dowody mechanicystyczne są ewidentne, albo co w sytuacji, gdy badania i na ludziach, i zwierzętach są, chociaż ograniczone, jednak nie widzimy mechanizmu? Wtedy – ponownie – zamiast opierać się na czyjejś opinii, opieramy się na Preambule, która mówi jasno, jak wygląda klasyfikacja. Jak w tabeli poniżej:
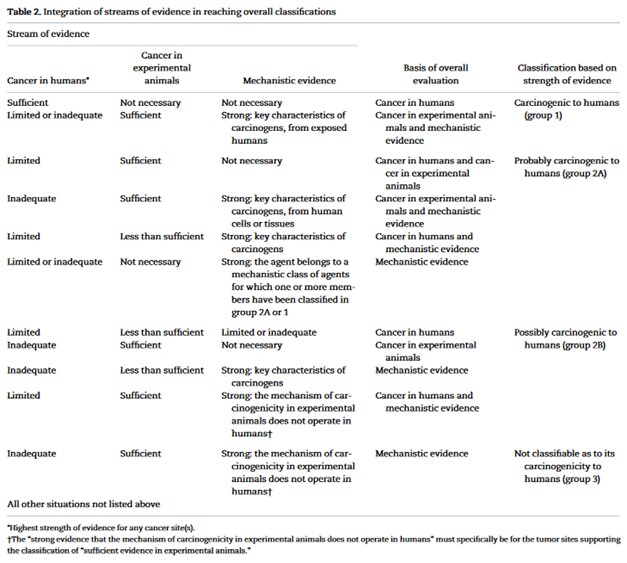
Trudno się w tym połapać? Dlatego właśnie do oceny „materiału dowodowego” w postaci publikacji zbiera się zespół roboczy ekspertów, który formuje się w długotrwałym i sformalizowanym procesie. Jego zwieńczeniem jest spotkanie tej grupy w Lyonie na bite osiem dni, aby wydyskutować na bazie dowodów konsensus. Później następuje publikacja w „The Lancet Oncology”, a na koniec zebranie wszystkiego do postaci monografii. Cały proces, od ogłoszenia, jakim czynnikiem IARC się zajmie, do publikacji monografii na ten temat, to niecałe dwa lata.
Co ważne, w ramach rozwoju wiedzy Preambuła była aktualizowana: w 1982 r, ponieważ wdrożono możliwość ewaluacji krótkoterminowej genotoksyczności, w 1991 r., aby podkreślić rolę mechanizmów i w 2006 r., aby jeszcze bardziej wzmocnić transparentność przez zarządzanie konfliktem interesów. Postawiono m.in. na sprecyzowanie różnych ról (członkowie grup roboczych, zaproszeni specjaliści, przedstawiciele, obserwatorzy, sekretariat IARC), zakaz czerpania korzyści z bycia w grupie, np. bycia konsultantem w sprawie ocenianego czynnika, transparentny i sformalizowany proces wyboru, selekcji i oceny, potem praca w podgrupach i prezentacja merytoryczna wyników, akceptowana przez większe grupy, aż całość osiągnie konsensus – indywidualne wpływy są zminimalizowane.
Prawdopodobnie czy być może?
Wydano do tej pory 131 monografii, co pozwoliło sklasyfikować 1035 czynników według poniższego schematu. Jeśli dane z badań na ludziach nie są wystarczające, to dwa pozostałe strumienie danych muszą dać spójny obraz, aby uznać, że coś faktycznie jest kancerogenne, czyli trafić do grupy 1. W przeciwnym wypadku otrzymuje status „prawdopodobnie” kancerogenne, czyli 2A, jeśli mamy ograniczone dane na ludziach, ale drugi ze strumieni daje nam dostateczny dowód. Jeśli natomiast mamy tylko jedno źródło dowodu – to uznajemy to za „być może” kancerogenne, czyli 2B. Każda inna sytuacja oznacza grupę trzecią.

W efekcie co do 121 z nich nie mamy wątpliwości, że są kancerogenne. Natomiast w wielu przypadkach badania wciąż trwają, ponieważ obecne dowody nie są wystarczające, przez co w grupie drugiej mamy odpowiednio 93 czynniki sklasyfikowane jako 2A i 320 jako 2B. Pozostaje czekać na dalsze aktualizacje.

Uwaga końcowa
Podczas ostatniej aktualizacji Preambuły dokonano jeszcze jednej istotnej zmiany… w nazwie monografii. Od tego momentu oficjalny tytuł opracowań to „IARC Monographs on the Identification of Carcinogenic Hazards to Humans”. Rzecz sprowadza się do rozróżnienia słowa „hazard” od „risk”. IARC podkreśla, że nie zajmuje się oceną ryzyka (wysokie? niskie?), ale samym faktem istnienia możliwości wywołania raka u ludzi, niezależnie od prawdopodobieństwa zajścia takiego zdarzenia! Ale o tym w kolejnej części, poświęconej już ściśle Monografii numer 102, czyli polom elektromagnetycznym.
Źródła:
The IARC Monographs: Updated Procedures for Modern and Transparent Evidence Synthesis in Cancer Hazard Identification, Jonathan M Samet et al., JNCI: Journal of the National Cancer Institute, Volume 112, Issue 1, January 2020, Pages 30–37, https://doi.org/10.1093/jnci/djz169 Published: 09 September 2019
https://academic.oup.com/jnci/article/112/1/30/5566248
International Agency for Research on Cancer: The first 50 years, 1965–2015. The History of IARC. Authors: Saracci R, Wild CP
Agents Classified by the IARC Monographs, Volumes 1–131
https://monographs.iarc.who.int/agents-classified-by-the-iarc/